Biofármaco desenvolvido pela UFRJ está na fase 1 de estudos clínicos e ainda depende de aprovação da Anvisa
Uma molécula desenvolvida no Brasil reacendeu a esperança de pacientes com lesão medular ao apresentar resultados promissores na recuperação de movimentos. A polilaminina, biofármaco criado por pesquisadores da Universidade Federal do Rio de Janeiro, é apontada como um dos avanços mais relevantes na área, mas ainda precisa passar por etapas rigorosas antes de chegar ao mercado.
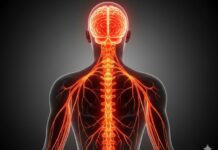
A substância é uma reconstrução da laminina, proteína presente naturalmente no organismo de diversos animais — inclusive na placenta humana — e atua na regeneração da medula espinhal em casos de lesão. A pesquisa é coordenada pela bioquímica Tatiana Sampaio e está em desenvolvimento há 27 anos.
Embora ao menos três pacientes tenham apresentado melhora, especialistas alertam que casos isolados não são suficientes para comprovar eficácia. O estudo foi autorizado pela Agência Nacional de Vigilância Sanitária e atualmente está na fase 1 dos ensaios clínicos.
Como funciona cada etapa
Antes de chegar aos testes em humanos, a polilaminina passou pela fase pré-clínica, quando foram analisados aspectos como toxicidade, mecanismo de ação, dose segura e possíveis efeitos colaterais em modelos experimentais.
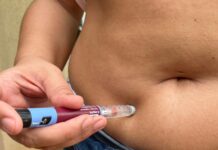
Agora, na fase 1, o foco é avaliar a segurança do tratamento em um grupo reduzido de participantes com lesão medular aguda. Nessa etapa, o objetivo principal não é comprovar eficácia, mas verificar se o medicamento não causa danos.
As próximas fases incluem:
- Fase 2: ampliação do número de participantes para avaliação inicial da eficácia e comparação de diferentes doses;
- Fase 3: estudos em larga escala, com centenas ou milhares de voluntários, para confirmar segurança e eficácia.
Após a conclusão das fases clínicas, os dados precisam ser apresentados à Anvisa, incluindo informações detalhadas sobre segurança, eficácia, processo de fabricação e controle de qualidade.
Além disso, é necessária uma Avaliação de Tecnologias em Saúde (ATS) pelo Ministério da Saúde para que o medicamento possa ser incorporado ao Sistema Único de Saúde.
Questão das patentes
Apesar de manter a patente no Brasil, a polilaminina perdeu o registro internacional após cortes de verbas na UFRJ em 2016, que impediram o pagamento das taxas de manutenção fora do país.
Para garantir proteção internacional, é necessário registrar o pedido no âmbito do PCT (Tratado de Cooperação em Matéria de Patentes), mecanismo que assegura prioridade temporária em vários países. Sem a manutenção desse registro, outras empresas podem explorar a tecnologia no exterior.
Especialistas apontam que a patente não é apenas um instrumento econômico, mas também estratégico para o desenvolvimento científico. Além de proteger a invenção, ela pode atrair investimentos privados e viabilizar a transferência de tecnologia.
Enquanto as etapas regulatórias seguem em andamento, a polilaminina permanece como uma promessa científica — cercada de expectativas, mas ainda dependente de comprovação definitiva para se tornar tratamento disponível à população.