Medicamento inovador depende de regulação de preço e análise da Conitec para distribuição gratuita
Tomar um medicamento apenas duas vezes por ano para prevenir o HIV pode parecer algo distante da realidade brasileira, mas essa possibilidade já foi aprovada pela Anvisa. O problema é que, mesmo após o aval da agência reguladora há mais de três meses, o lenacapavir ainda não tem data para chegar ao SUS — e o principal entrave, neste momento, é o preço.
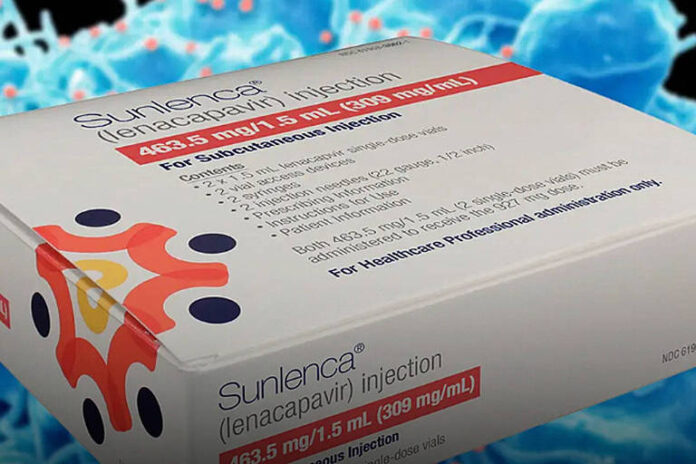
O medicamento, comercializado internacionalmente com o nome de Sunlenca, é uma injeção semestral usada como profilaxia pré-exposição ao HIV (PrEP). Estudos clínicos apontaram eficácia próxima de 100% na prevenção da infecção, colocando a tecnologia entre as mais promissoras já desenvolvidas contra o vírus.
Apesar disso, antes de qualquer discussão sobre distribuição gratuita no sistema público, o remédio precisa passar por uma etapa obrigatória: a definição do preço máximo pela Câmara de Regulação do Mercado de Medicamentos (CMED). Segundo a Anvisa, o prazo para conclusão dessa análise vai até 3 de junho, caso não haja interrupções técnicas.
A farmacêutica Gilead Sciences, responsável pelo medicamento, protocolou o pedido de precificação em março. Somente após essa etapa o lenacapavir poderá ser analisado pela Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec), órgão que avalia eficácia, segurança e custo-benefício de novos tratamentos antes de recomendar ou não sua incorporação ao sistema público.
Em nota, o Ministério da Saúde informou que o medicamento ainda não pode ser amplamente comercializado no Brasil justamente por não ter o preço regulamentado.
Hoje, o maior desafio para a chegada do lenacapavir ao SUS é o custo elevado. Nos Estados Unidos, o tratamento pode ultrapassar US$ 25 mil por pessoa ao ano — o equivalente a cerca de R$ 136 mil. Em alguns casos, o valor chega a quase R$ 241 mil anuais.
Para o infectologista Rico Vasconcelos, pesquisador do Hospital das Clínicas da Faculdade de Medicina da USP, a eficácia do medicamento representa um avanço importante, mas o impacto financeiro torna inviável uma adoção ampla no sistema público neste momento.
“O principal limitante é o preço. O lenacapavir representa um grande avanço tecnológico, mas ainda precisamos entender como seria a implementação em larga escala no SUS”, avalia.
O Brasil ficou fora dos acordos internacionais firmados pela Gilead para produção de versões genéricas do medicamento. Os contratos contemplam 120 países considerados economicamente mais vulneráveis, o que pode dificultar negociações futuras para redução de custos.
Mesmo assim, especialistas destacam que o país possui histórico de negociações bem-sucedidas envolvendo medicamentos contra HIV e aids desde os anos 1990. Em janeiro deste ano, a farmacêutica assinou um memorando de entendimento com Farmanguinhos/Fiocruz para avaliar possíveis formas de cooperação e eventual produção nacional no futuro.
Enquanto a incorporação ao SUS não avança, o Brasil já começou a testar o uso do medicamento na prática. O estudo ImPrEP LEN Brasil, coordenado pela Fiocruz, está em andamento em sete cidades brasileiras, incluindo São Paulo, Rio de Janeiro, Salvador e Manaus.
A pesquisa acompanha 1.500 participantes para entender como o medicamento funciona na rotina real dos serviços de saúde. O público-alvo inclui gays, bissexuais, homens trans, mulheres trans e pessoas não-binárias entre 16 e 30 anos.
O lenacapavir é aplicado apenas duas vezes por ano, ao contrário da PrEP oral tradicional, que exige comprimidos diários. A proposta é facilitar a adesão à prevenção, principalmente entre pessoas que têm dificuldade em manter o uso contínuo da medicação.
Atualmente, cerca de 150 mil pessoas utilizam a PrEP no Brasil pelo SUS. Especialistas afirmam, no entanto, que o lenacapavir não substituiria os comprimidos já disponíveis, mas funcionaria como uma alternativa complementar dentro da estratégia de prevenção combinada.
A Organização Mundial da Saúde (OMS) já passou a recomendar o medicamento como uma das principais opções disponíveis para prevenção do HIV enquanto não existe uma vacina contra o vírus.
Nos estudos mais recentes, nenhuma das mais de 2 mil mulheres que receberam a aplicação do lenacapavir contraiu HIV durante os testes clínicos realizados na África do Sul e em Uganda. Resultados semelhantes também foram registrados em pesquisas feitas com homens cis, homens trans e pessoas não-binárias em países como Brasil, México e Estados Unidos.
Além da eficácia elevada, o medicamento atua de maneira inovadora. Em vez de atacar apenas uma etapa da infecção, o lenacapavir interfere no capsídeo do HIV — estrutura que protege o material genético do vírus — dificultando sua multiplicação no organismo.
Apesar do entusiasmo da comunidade científica, especialistas avaliam que uma eventual adoção no SUS deverá ocorrer de forma gradual e direcionada a grupos prioritários, especialmente pessoas com maior dificuldade de adesão à PrEP oral diária.
Até lá, o avanço do medicamento no Brasil dependerá das próximas decisões regulatórias e, principalmente, das negociações sobre preço e viabilidade econômica para o sistema público de saúde.